第二节 个别氨基酸代谢
某些氨基酸在代谢过程中能生成含一个碳原子的基团,经过转移参与生物合成过程。这些含一个碳原子的基团称为一碳单位(C1unit或one carbon unit)。有关一碳单位生成和转移的代谢称为一碳单位代谢。
体内的一碳单位有:甲基(-CH3,methyl)、甲烯基(-CH2??,methylene),甲炔基(-CH=,methenyl)、甲酰基(-CHO,formyl)及亚氨甲基(-CH=NH,formimino)等。它们可分别来自甘氨酸、组氨酸、丝氨酸、色氨酸、蛋氨酸等(图7-12)。
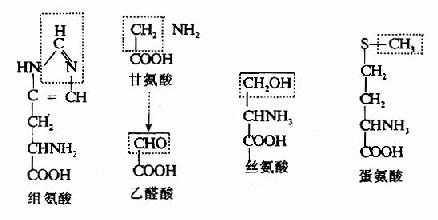
图7-12 一碳单位的来源
(一)一碳单位代酸的辅酶
一碳单位不能游离存在,通常与四氢叶酸(Tetrahydrofolic acid,FH4)结合而转运或参加生物代谢,FH4是一碳单位代谢的辅酶。
四氢叶酸由叶酸(folicacid)衍生而来。叶酸需经二次还原方可转变为活性辅酶形式-FH4(图7-13)。两次还原均由二氢叶酸还原酶(dihyclrofolatereductase)所催化。
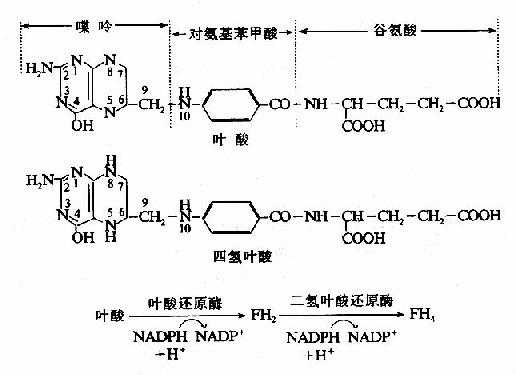
图7-13 四氢叶酸的生成
一碳单位共价连接于FH4分子的N5、N10位或N5和N10位上。
(二)一碳单位的来源及转换
一碳单位主要来源于丝氨酸,在丝氨酸羟甲基转移酶催化为甘氨酸过程中产生的N5,N10?布紫┆?FH4;甘氨酸在甘氨酸合成酶(glycine synthase)催化下可分解为CO2,NH+4和N5,N10?CH2?FH4。此外,苏氨酸和丝氨酸都可经相应酶催化转变为丝氨酸。因此亦可产生N5、N10?CH2?FH4。
在组氨酸转变为谷氨酸过程中由亚胺甲基谷氨酸提供了N5?CH=NH??FH4。
色氨酸分解代谢能产生甲酸,甲酸可与FH4结合产生N10?CHO?FH4。
体内一碳单位分别处于甲酸、甲醛不同的氧化水平,在相应的酶促氧化还原反应下可相互转换(图7-14)。这些反应中,N5-CH3-FH4的生成基本是不可逆的。N5-CH3?FH4可将甲基转移给同型半胱氨酸生成蛋氨酸和FH4。催化此反应的酶是N5-CH3FH4同型半胱氨酸甲基转移酶,辅酶为甲基B12。此反应不可逆,故N5-CH3FH4不能自蛋氨酸生成。
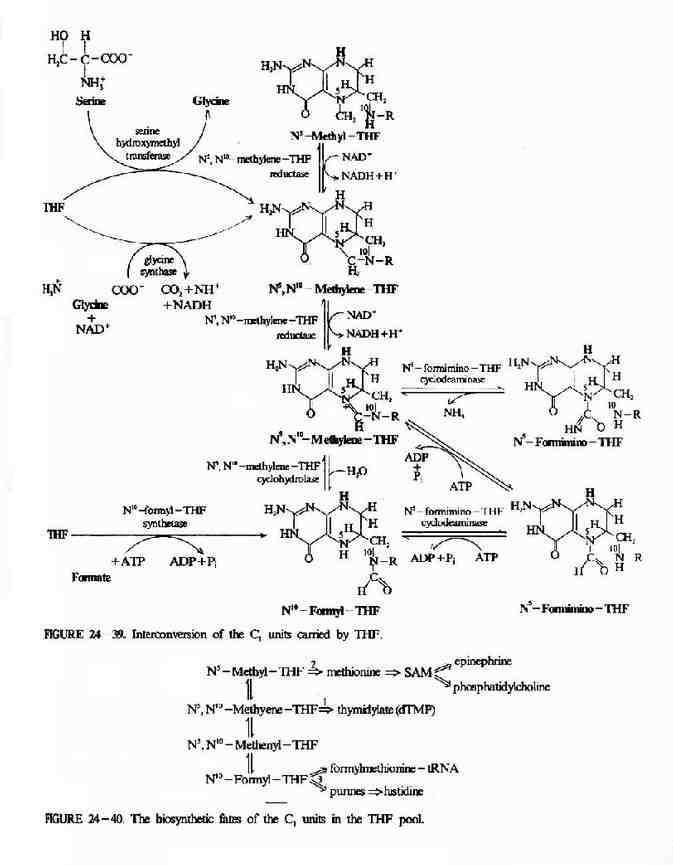
图7-14 一碳单位的相互转化
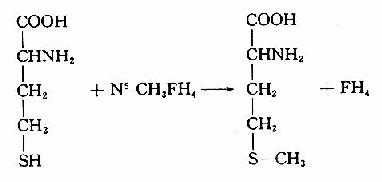
蛋氨酸分子中的甲基也是一碳单位。在ATP的参与下蛋氨酸转变生成S-腺苷蛋氨酸(Sadenosylmethionine,又称活性蛋氨酸)。S?蚕佘盏鞍彼崾腔钇玫募谆?供体。因此四氢叶酸并不是一碳单位的唯一载体。

(三)一碳单位的功能
1.一碳单位是合成嘌呤和嘧啶的原料,在核酸生物合成中有重要作用。如N5-N10-CH=FH4直接提供甲基用子脱氧核苷酸dUMP向dTMP的转化。N10-CHO-FH4和N5N10-CH=FH4分别参与嘌呤碱中C2,C3原子的生成。
2.SAM提供甲基可参与体内多种物质合成。例如肾上腺素、胆碱、胆酸等。
一碳单位代谢将氨基酸代谢与核苷酸及一些重要物质的生物合成联系起来。一碳单位代谢的障碍可造成某些病理情况,如巨幼红细胞贫血等。磺胺药及某抗癌药(氨甲喋呤等)正是分别通过干扰细菌及瘤细胞的叶酸、四氢叶酸合成,进而影响核酸合成而发挥药理作用的。
含硫氨基酸共有蛋氨酸、半胱氨酸和胱氨酸三种,蛋氨酸可转变为半胱氨酸和胱氨酸,后两者也可以互变,但后者不能变成蛋氨酸,所以蛋氨酸是必需氨基酸。
(一)蛋氨酸代谢
1.转甲基作用与蛋氨酸循环 蛋氨酸中含有S甲基,可参与多种转甲基的反应生成多种含甲基的生理活性物质。在腺苷转移酶催化下与ATP反应生成S-腺苷蛋氨酸(S-adenosglmethiomine,SAM)。SAM中的甲基是高度活化的,称活性甲基,SAM称为活性蛋氨酸。
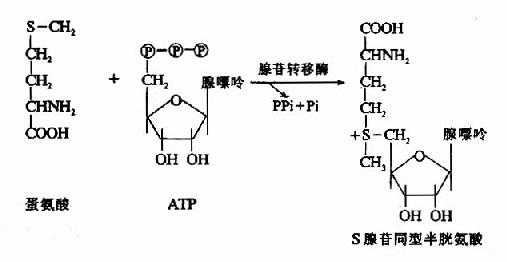
SAM可在不同甲基转移酶(methyl transferase)的催化下,将甲基转移给各种甲接受体而形成许多甲基化合物,如肾上腺素、胆碱、甜菜碱、肉毒碱、肌酸等都是从SAM中获得甲基的。SAM是体内最主要的甲基供体。
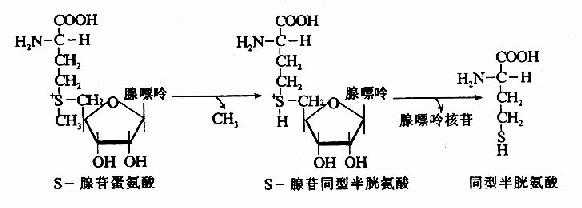
SAM转出甲基后形成S?蚕佘胀?型半胱氨酸S??adenosylhomocystine,SAH),SAH水解释出腺苷变为同型半胱氨酸(homocystine,hCys)。同型半胱氨酸可以接受N5?CH3?HF4提供的甲基再生成蛋氨酸,形成一个循环过程,称为蛋氨酸循环(methionine cycle)。此循环的生理意义在于蛋氨酸分子中甲基可间接通过N5?CH3?FH4由其它非必需氨基酸提供,以防蛋氨酸的大量消耗(图7-15)。
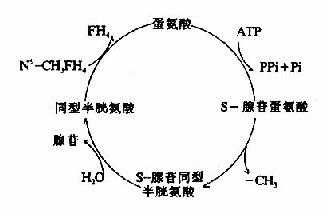
图7-15 S-腺苷蛋氨酸循环
N5-CH3FH4同型半胱氨酸甲基转移酶的辅酶是甲基B12。维生素B12缺乏会引起蛋氨酸循环受阻。临床上可以见到维生素B12缺乏引起的巨幼细胞性贫血。1962年Noronha与Silverman首先提出了甲基陷阱学说(methyl-trap hypothesis),后来Herbert与Zaulsky又作了修改。这个学说认为:由于维生素B12缺乏,引起甲基B12缺乏,使甲基转移酶活性低下,甲基转移反应受阻导致叶酸以N5-CH3FH4形式在体内堆积。这样,其它形式的叶酸大量消耗,以这些叶酸作辅酶的酶活力降低,影响了嘌呤碱和胸腺嘧啶的合成,因而影响核酸的合成,引起巨幼细胞性贫血。也就是说,维生素B12对核酸合成的影响是间接地通过影响叶酸代谢而实现的。
虽蛋氨酸循环可生成蛋氨酸,但体内不能合成同型半胱氨酸,只能由蛋氨酸转变而来,所以体内实际上不能合成蛋氨酸,必须由食物供给。
同型半胱氨酸还可在胱硫醚合成酶(cystathiorinesynthase)催化下与丝氨酸缩合生成胱硫醚(cystathionine),再经胱硫醚酶催化水解生成半胱氨酸,α-酮丁酸和氨。α-酮丁酸转变为琥珀酸单酰CoA,通过三羧酸循环,可以生成葡萄糖、所以蛋氨酸为生糖氨基酸。
2.肌酸的合成 肌酸(creatine)和磷酸肌酸(creatinephosphate)在能量储存及利用中起重要作用。二者互变使体内ATP供应具有后备潜力。肌酸在肝和肾中合成,广泛分布于骨骼肌、心肌、大脑等组织中。肌酸以甘氨酸为骨架,精氨酸提供脒基、SAM供给甲基、在脒基转移酶和甲基转移酶的催化下合成。在肌酸激酶(creatinephosphohinase,CPK)催化下将ATP中?P转移到肌酸分子中形成磷酸肌酸(CP)储备起来(图7-16)。
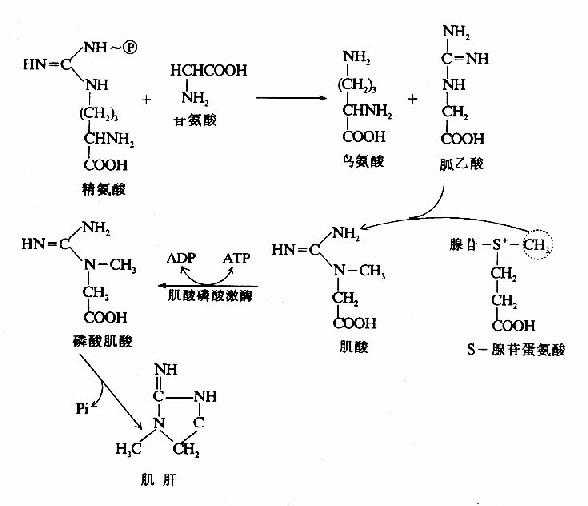
图7-16 肌酸的代谢
CPK由两种亚基组成;即M亚基(肌型)与B亚基(脑型)。有三种同工酶;即MM型(在骨骼肌中)BB型在脑中)和MB型(在心肌中)。心肌梗塞时,血中MB型CPK活性增高,可作辅助诊断的指标之一。
肌酸和磷酸肌酸代谢的终产物是肌酸酐(creatinine)简称肌酐。正常成人,每日尿中肌酐量恒定。肾功能障碍时,检查血或尿中肌酐含量以帮助诊断。
(二)半胱氨酸和胱氨酸的代谢
1.半胱氨酸和胱氨酸的互变 半胱氨酸含巯基(-SH),胱氨酸含有二硫键(S-S-),二者可通过氧化还原而互变。胱氨酸不参与蛋白质的合成,蛋白质中的胱氨酸由半胱氨酸残基氧化脱氢而来。在蛋白质分子中两个半胱氨酸残基间所形成的二硫键对维持蛋白质分子构象起重要作用。而蛋白分子中半胱氨酸的巯基是许多蛋白质或酶的活性基团。
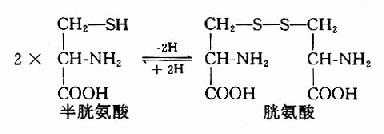
2.半胱氨酸分解代谢 人体中半胱氨酸主要通过两条途径降解为丙酮酸。一是加双氧酶催化的直接氧化途径,或称半胱亚磺酸途径,另一是通过转氨的3-巯基丙酮酸途径。
3.活性硫酸根代谢 含硫氨基酸经分解代谢可生成H2S,H2S氧化成为硫酸。半胱氨酸巯基亦可先氧化生成亚磺基,然后再生成硫酸。其中一部分以无机盐形式从尿中排出,一部分经活化生成3′磷酸腺苷-5'-磷酸硫酸(3'-phosphoadenosine??5'-phosphosulfate,PAPS),即活性硫酸根。
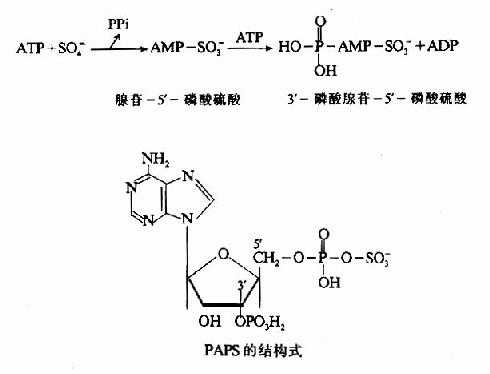
PAPS的性质活泼,在肝脏的生物转化中有重要作用。例如类固醇激素可与PAPS结合成硫酸酯而被灭活,一些外源性酚类亦可形成硫酸酯而增加其溶解性以利于从尿于排出。此外,PAPS也可参与硫酸角质素及硫酸软骨素等分子中硫酸化氨基多糖的合成。
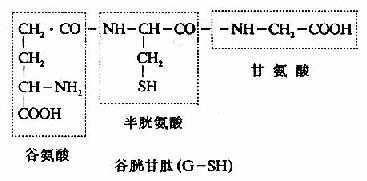
4.谷胱甘肽的合成 谷胱甘肽(glutathiose,r??glutamylcysteinglglycine,GSH)是一种?ず?γ-酰胺键的三肽,由谷氨酸、半胱氨酸及甘氨酸组成。GSH的合成通过γ-谷氨酰基循环(γ-glutamyl cycle),由Meister提出,又称为Meister循环(图7-17)。γ-谷氨酰基循环有双重作用,一是GSH的再合成,二是通过GSH的合成与分解将外源氨基酸主动转运到细胞内。
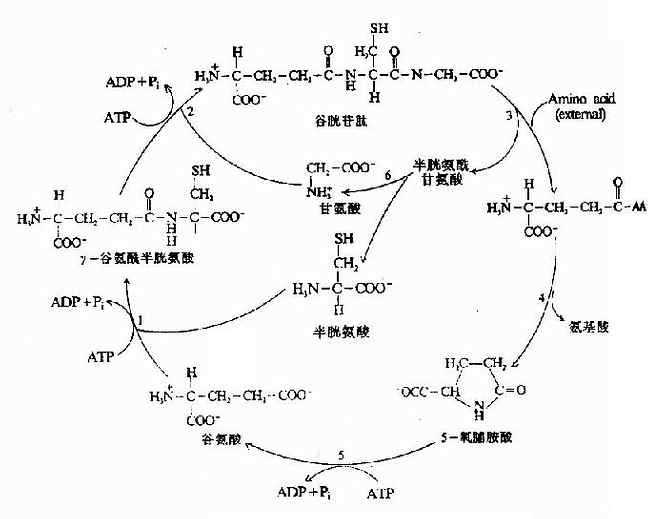
图7-17 γ-谷氨酰基循环
GSH的合成由γ-谷氨酰半胱氨酸合成酶(γ-glutamylcysteinsynthetase)和GSH合成酶(GSHsynthetase)所催化。由ATP水解供能。GSH的分解中γ-谷氨酰转肽酶(γ-glutamyl transpeptidase)、γ-谷氨酰环转移酶(γ-gltamyl cyclotransforase)和5氧脯氨酸酶(5oxoprolinase)及一个细胞内肽酶(protease)所催化。
GSH在人体解毒、氨基酸转运及代谢中均有重要作用。GSH的活性基团是其半胱氨酸残基上的巯基,GSH有氧化型和还原型两种形式,可以互变。
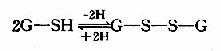
谷胱甘胱还原酶催化上面反应,辅酶为NADPH,细胞中GSH与GSSG的比例为100:1。GSH可保护某些蛋白质及酶分子的巯基不被氧化,从而维持其生物活性。如红细胞中含有较多GSH,对保护红细胞膜完整性及促使高铁血红蛋白还原为血红蛋白均有重要作用。此外,体内产生的过氧化物及自由基,亦可通过含硒的GSH过氧化酶而被清除,如:

芳香族氨基酸包括苯丙氨酸,酪氨酸和色氨酸,苯丙氨酸和酪氨酸结构相似,在体内苯丙氨酸可转变成酪氨酶,所以合并在一起讨论。
(一)苯丙氨酸和酪氨酸
1.苯丙氨酸在体内一般先转变为酪氨酸。由苯丙氨酸羟化酶(phenylalamine hyolroxylase)催化引入羟基完成,其辅酶为四氢生物嘌呤。反应生成的二氢生物喋呤,由二氢叶酸还原酶催化,借助NADPH+H还原为四氢化合物(图7-18)。
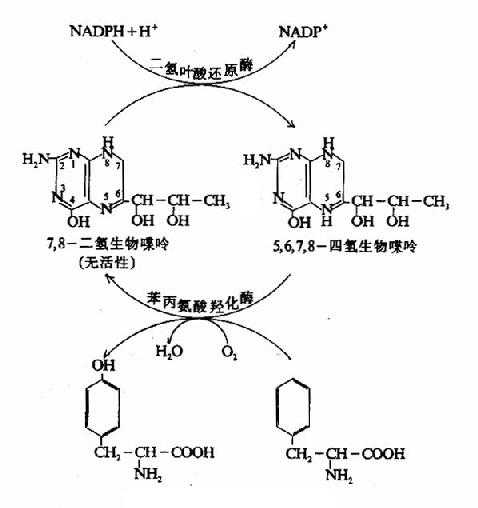
图7-18 酪氨酸的生成
苯丙氨酸羟化酶所催化反应不可逆,体内酷氨酸不能转变为苯丙氨酸。
2.儿茶酚胺与黑色素的合成 酪氨酸经酪氨酸羟化酶(tyrosine hydroxylase)催化生成3,4二羟苯丙氨酸(3,4dihydroxyphenylalanineL-DOPA)(多巴)。此酶也是以四氢生物喋呤为辅酶的加单氧酶,多巴经多巴脱羧酶催化生成多巴胺(dopamine)。多巴胺在多巴胺β-氧化酶(dopamine β??oxidase)催化下使β碳原子羟化,生成去甲肾上腺素(norepinephrine)。而后由SAM提供甲基使去甲肾上腺素甲基化生成肾上腺素(epinephrine)。多巴胺、去甲肾上腺素、肾上腺素统称为儿茶酚胺(catecholamine)。酪氨酸羟化酶是儿茶酚胺合成的限速酶,受终产物的反馈调节(图7-19)。
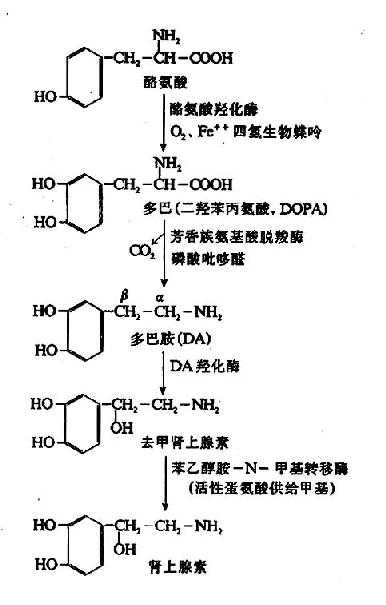
图7-19 儿茶酚胺的合成
在黑色素细胞中,酪氨酸在酪氨酸酶催化下羟化生成多巴,多巴再经氧化生成多巴醌而进入合成黑色素的途径。所形成的多巴醌进一步环化和脱羧生成吲哚醌。黑色素即是吲哚醌的聚合物。人体若缺乏酪氨酸酶,黑色素合成障碍,皮肤、毛发发“白”,称为白化病(albinism)(图7-20)。
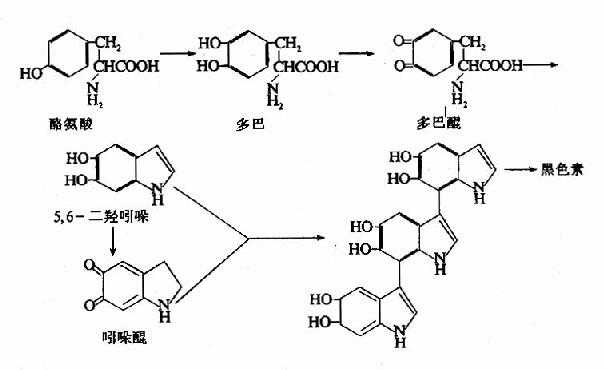
图7-20 黑色素的生成
3.酪氨酸是生糖兼生酮氨基酸 酪氨酸经转氨基作用生成对羟基苯丙酮酸,进一步分解则生成乙酰乙酸和延胡索酸,所以是生糖兼生酮氨基酸。
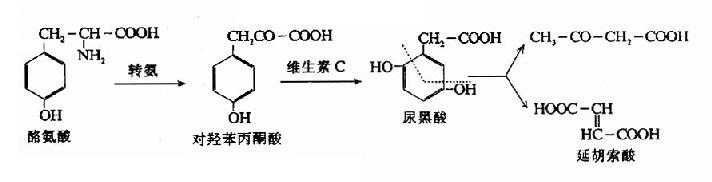
4.代谢障碍 已知在苯丙氨酸和酪氨酸代谢中,有许多代谢性疾患。最重要的是苯丙酮酸尿症(phenylketonuria,PKV),因缺乏苯丙氨酸羟化酶所致。苯丙氨酸不能正常地转变为酪氨酸,体内苯丙氨酸蓄积,并由转氨基作用生成苯丙酮酸(一部分还原为苯乙酸)并从尿液中排出。苯丙酮酸的堆积对中枢神经系统有毒性,故本病伴发智力发育障碍。早期发现时可控制饮食中苯丙氨酸含量,有利于智力发育。
另一代谢疾患为尿黑酸尿症(alkaptonuria)。酪氨酸在分解代谢中生成中间产物尿黑酸,如尿黑酸氧化酶缺乏,则尿黑酸裂环降解受阻,大量尿黑酸排入尿中,经空气氧化为相应的对醌,后者可聚合为黑的色素。此种代谢性疾患一般无严重后果。
此外,巴金森病(Parkinson′sdisease)是由于脑生成多巴胺的功能退化所致的一种严重的神经系统疾病。临床常用L?捕喟椭瘟疲?L-多巴本身不能通过血?材云琳衔拗苯恿菩В?但在相应组织中脱羧可生成多巴胺达到治疗作用。目前,采用将大脑中植移肾上腺髓质,借此生成多巴胺以弥补脑中多巴胺不足,取得较好疗效。
(二)色氨酸的代谢
色氨酸是必需氨基酸。大多数蛋白质中含量均较少,机体对其摄取少,分解亦少。除参加蛋白质合成外,还可经氧化脱羧生成5?掺巧?胺(前述)。并可降解产生生糖,生酮成分,此过程中产生一碳单位及尼克酸等。
1.色氨酸分解首先在色氨酸-2,3-加双氧酶(tryptophan-2,3-dioxygenase)作用下将吡酪环打开,生成N-甲酰犬尿氨酸(N-Formylkynurenine)。此酶辅基为铁卟啉,Vit C有保护辅基中Fe2+不被氧化的作用,亦可说Vit C是此酶的激活剂。在甲酰化酶(formamidase)的作用下,甲酰犬尿氨酸脱甲酰基生成甲酸和犬尿氨酸,甲酸可参加一碳单位代谢。而犬尿氨酸则有三个不同代谢方向。
(1)犬尿氨酸主要由犬尿氨酸羟化酶(Rynurenine-3-monoxygenase)催化生成3?掺侨?尿氨酸(3-hydroxykynurenine),而后由犬尿氨酸酶(kynureninase)(以PLP为辅酶)催化水解裂出丙氨酸,并生成了3-羟邻氨苯甲酸(3-hydroxyanthranilate),丙氨酸可经转氨生成丙酮酸,而3-羟邻苯甲酸经氧化裂环,脱羧等反应生成α?餐?乙酸,进而生成乙酰乙酸。因此,色氨酸为生糖兼生酮氨基酸。
(2)少量犬尿氨酸经转氨作用并缩合生成犬尿酸。
(3)少量裂解出丙氨酸后生成邻氨苯甲酸。
2.尼克酸的生成 色氨酸分解代谢中的3-羟邻氨苯甲酸经3-羟邻氨苯丙酸-3,4,-加双氧酶(3-hydroxyanthranilate-3,4-dioxygenase)催化裂环,可生成尼克酸,是构成NAD(P)+的关键成分。这是体内合成维生素的一个特例。
支链氨基酸(branched??amino acid,BCAA)包括亮氨酸、异亮氨酸和缬氨酸。三者均为必需氨基酸。分解代谢主要在肌肉组织中进行。它们分属于三类,亮氨酸为生酮氨基酸,缬氨酸为生糖氨基酸,异亮氨酸为生糖兼生酮氨基酸。
三种支链氨基酸分解代谢过程均较复杂,一般可分为二阶段。第一阶段,三种氨基酸前三步反应性质相同,产物类似。均为CoA的衍生物,可称为共同反应阶段。第二阶段则反应各异,经若干步反应,亮氨酸产生乙酰CoA及乙酰乙酰CoA,缬氨酸产生琥珀酸单酰CoA,异亮氨酸产生乙酰CoA及琥珀酸单酰CoA分别纳入生糖或生酮的代谢(图7-21)。

图7-21 支链氨基酸的分解代谢

《生物化学与分子生物学》相关章节:
- ……
- 第一节 概 述
- 第二节 呼 吸 链
- 第三节 ATP的生成、储存和利用
- 第七章 氨基酸代谢
- 第一节 氨基酸的一般代谢
- 第二节 个别氨基酸代谢(当前内容)
- 第三节 氨基酸的生物合成
- 第八章 核苷酸代谢(Nucleotide Metabo lism)
- 第一节 核苷酸的化学结构
- 第二节 嘌呤核苷酸的合成代谢
- ……







