第四节 脂肪酸代谢
脂肪酸在有充足氧供给的情况下,可氧化分解为CO2和H2O,释放大量能量,因此脂肪酸是机体主要能量来源之一。肝和肌肉是进行脂肪酸氧化最活跃的组织,其最主要的氧化形式是β-氧化。
此过程可分为活化,转移,β-氧化共三个阶段。
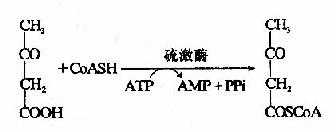
1.脂肪酸的活化
和葡萄糖一样,脂肪酸参加代谢前也先要活化。其活化形式是硫酯:脂肪酰CoA,催化脂肪酸活化的酶是脂酰CoA合成酶(acyl CoA synthetase)。

活化后生成的脂酰CoA极性增强,易溶于水;分子中有高能键、性质活泼;是酶的特异底物,与酶的亲和力大,因此更容易参加反应。
脂酰CoA合成酶又称硫激酶,分布在胞浆中、线粒体膜和内质网膜上。胞浆中的硫激酶催化
中短链脂肪酸活化;内质网膜上的酶活化长链脂肪酸,生成脂酰CoA,然后进入内质网用于甘油三酯合成;而线粒体膜上的酶活化的长链脂酰CoA,进入线粒体进入β-氧化。
2.脂酰CoA进入线粒体:催化脂肪酸β-氧化的酶系在线粒体基质中,但长链脂酰CoA不能自由通过线粒体内膜,要进入线粒体基质就需要载体转运,这一载体就是肉毒碱(carnitine),即3-羟-4-三甲氨基丁酸。
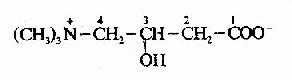
长链脂肪酰CoA和肉毒碱反应,生成辅酶A和脂酰肉毒碱,脂肪酰基与肉毒碱的3?掺腔?通过酯键相连接。
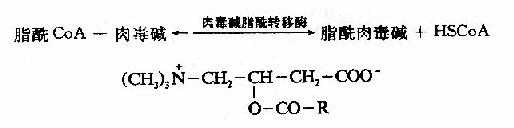
催化此反应的酶为肉毒碱脂酰转移酶(carnitineacyl transferase)。线粒体内膜的内外两侧均有此酶,系同工酶,分别称为肉毒碱脂酰转移酶I和肉毒碱脂酰转移酶Ⅱ。酶Ⅰ使胞浆的脂酰CoA转化为辅酶A和脂肪酰肉毒碱,后者进入线粒体内膜。位于线粒体内膜内侧的酶Ⅱ又使脂肪酰肉毒碱转化成肉毒碱和脂酰CoA,肉毒碱重新发挥其载体功能,脂酰CoA则进入线粒体基质,成为脂肪酸β-氧化酶系的底物(图5-10)。

图5-10 肉毒碱参与脂酰辅酶A转入线粒体示意图
酶Ⅰ:位于线粒体内膜外侧的肉毒碱脂酰转移酶
酶Ⅱ:位于线粒体内膜内侧的肉毒碱脂酰转移酶
长链脂酰CoA进入线粒体的速度受到肉毒碱脂酰转移酶Ⅰ和酶Ⅱ的调节,酶Ⅰ受丙二酰CoA抑制,酶Ⅱ受胰岛素抑制。丙二酰CoA是合成脂肪酸的原料,胰岛素通过诱导乙酰CoA羧化酶的合成使丙二酰CoA浓度增加,进而抑制酶Ⅰ。可以看出胰岛素对肉毒碱脂酰转移酶Ⅰ和酶Ⅱ有间接或直接抑制作用。饥饿或禁食时胰岛素分泌减少,肉毒碱脂酰转移酶Ⅰ和酶Ⅱ活性增高,转移的长链脂肪酸进入线粒体氧化供能。
3.β-氧化的反应过程:脂酰CoA在线粒体基质中进入β氧化要经过四步反应,即脱氢、加水、再脱氢和硫解,生成一分子乙酰CoA和一个少两个碳的新的脂酰CoA。
第一步脱氢(dehydrogenation)反应由脂酰CoA脱氢酶活化,辅基为FAD,脂酰CoA在α和β碳原子上各脱去一个氢原子生成具有反式双键的α、β-烯脂肪酰辅酶A。

第二步加水(hydration)反应由烯酰CoA水合酶催化,生成具有L-构型的β-羟脂酰CoA。
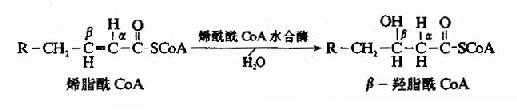
第三步脱氢反应是在β-羟脂肪酰CoA脱饴酶(辅酶为NAD+)催化下,β-羟脂肪酰CoA脱氢生成β酮脂酰CoA。
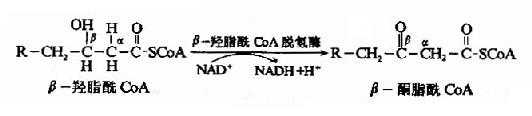
第四步硫解(thiolysis)反应由β-酮硫解酶催化,β-酮酯酰CoA在α和β碳原子之间断链,加上一分子辅酶A生成乙酰CoA和一个少两个碳原子的脂酰CoA。
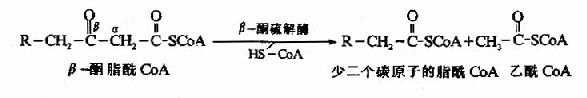
上述四步反应与TCA循环中由琥珀酸经延胡索酸、苹果酸生成草酰乙酸的过程相似,只是β-氧化的第四步反应是硫解,而草酰乙酸的下一步反应是与乙酰CoA缩合生成柠檬酸。
长链脂酰CoA经上面一次循环,碳链减少两个碳原子,生成一分子乙酰CoA,多次重复上面的循环,就会逐步生成乙酰CoA。
从上述可以看出脂肪酸的β-氧化过程具有以下特点。首先要将脂肪酸活化生成脂酰CoA,这是一个耗能过程。中、短链脂肪酸不需载体可直拉进入线粒体,而长链脂酰CoA需要肉毒碱转运。β-氧化反应在线粒体内进行,因此没有线粒体的红细胞不能氧化脂肪酸供能。β-氧化过程中有FADH2和NADH+H+生成,这些氢要经呼吸链传递给氧生成水,需要氧参加,乙酰CoA的氧化也需要氧。因此,β-氧化是绝对需氧的过程。
脂肪酸β-氧化的整个过程可用下图(图5-11)表示:

图5-11 脂肪酸β氧化反应过程
脂肪酸β-氧化是体内脂肪酸分解的主要途径,脂肪酸氧化可以供应机体所需要的大量能量,以十八个碳原子的饱和脂肪酸硬脂酸为例,其β-氧化的总反应为:
CH3(CH2)15COSCoA+8NAD++*CoASH+8H2O——→9CH3COSCoA+8FADH2+8NADH+8H+
8分子FADH2提供8×2=16分子ATP,8分子NADH+H+提供8×3=24分子ATP,9分子乙酰CoA完全氧化提供9×12=108个分子ATP,因此一克分子硬脂酸完全氧化生成CO2和H2O,共提供148克分子ATP。硬脂酸的活化过程消耗2克分子ATP,所以一克分子硬脂酸完全氧化可净生成146克分子ATP。一克分子葡萄糖完全氧化可生成38分子ATP。三克分子葡萄糖所含碳原子数与一克分子硬脂酸相同,前者可提供114克分子ATP,后者可提供146克分子ATP。可见在碳原子数相同的情况下脂肪酸能提供更多的能量。脂肪酸氧化时释放出来的能量约有40%为机体利用合成高能化合物,其余60%以热的形式释出,热效率为40%,说明人体能很有效地利用脂肪酸氧化所提供的能量。
脂肪酸β-氧化也是脂肪酸的改造过程,人体所需要的脂肪酸链的长短不同,通过β-氧化可将长链脂肪酸改造成长度适宜的脂肪酸,供机体代谢所需。
脂肪酸β-氧化过程中生成的乙酰CoA是一种十分重要的中间化合物,乙酰CoA除能进入三羧酸循环氧化供能外,还是许多重要化合物合成的原料,如酮体、胆固醇和类固醇化合物。
1.丙酸的氧化:人体内和膳食中含极少量的奇数碳原子脂肪酸,经过β-氧化除生成乙酰CoA外还生成一分子丙酰CoA,某些氨基酸如异亮氨酸、蛋氨酸和苏氨酸的分解代谢过程中有丙酰CoA生成,胆汁酸生成过程中亦产生丙酰CoA。丙酰CoA经过羧化反应和分子内重排,可转变生成琥珀酰CoA,可进一步氧化分解,也可经草酰乙酸异生成糖,反应过程见下图。
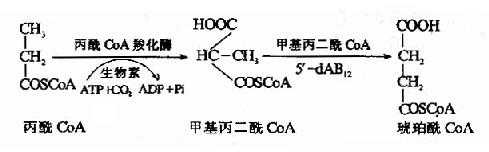
甲基丙二酰CoA变位酶的辅酶是5′-脱氧腺苷B12(5′dAB12),维生素B12缺乏或5′-dAB12生成障碍均影响变位酶活性,使甲基丙二酰CoA堆积。结果,一方面甲基丙二酰CoA脱去辅酶A,生成甲基丙二酸引起血中甲基丙二酸含量增高(甲基丙二酸血症),并从尿中排出体外(24小时排出量大于4mg时称为甲基丙二酸尿症)。另一方面又引起丙酰CoA浓度增高,可参与神经髓鞘脂类合成,生成异常脂肪酸(十五碳、十七碳和十九碳脂肪酸),引起神经髓鞘脱落、神经变性(临床上称为亚急性合并变性症)。
2.ω-氧化:脂肪酸的ω-氧化是在肝微粒体中进行,由加单氧酶催化的。首先是脂肪酸的ω?蔡荚?子羟化生成ω-羧脂肪酸,再经ω醛脂肪酸生成α、ω-二羧酸,然后在α-端或ω-端活化,进入线粒体进入β-氧化,最后生成琥珀酰CoA。
3.α-氧化:脂肪酸在微粒体中由加单氧酶和脱羧酶催化生成α-羟脂肪酸或少一个碳原子的脂肪酸的过程称为脂肪酸的α-氧化。长链脂肪酸由加单氧酶催化、由抗坏血酸或四氢叶酸作供氢体在O2和Fe2+参与下生成α-羟脂肪酸,这是脑苷脂和硫脂的重要成分,α-羟脂肪酸继续氧化脱羧就生成奇数碳原子脂肪酸。α-氧化障碍者不能氧化植烷酸(phytanic acid,3、7、11、15-四甲基十六烷酸)。牛奶和动物脂肪中均有此成分,在人体内大量堆积便引起Refsum氏病。α-氧化主要在脑组织内发生,因而α-氧化障碍多引起神经症状。
4.不饱和脂肪酸(unsaturated fatty acid)的氧化:人体内约有1/2以上的脂肪酸是不饱和脂肪酸,食物中也含有不饱和脂肪酸。这些不饱和脂肪酸的双键都是顺式的,它们活化后进入β-氧化时,生成3?菜诚┲?酰CoA,此时需要顺??3反??2异构酶催化使其生成2?卜聪┲?酰CoA以便进一步反应。2?卜聪┲?酰CoA加水后生成D?拨?-羟脂酰CoA,需要β-羟脂酰CoA差向异构酶催化,使其由D?补剐妥?变成L?补剐停?以便再进行脱氧反应(只有L?拨?-羟脂酰CoA才能作为β-羟脂酰CoA脱氢酶的底物)。
不饱和脂肪酸完全氧化生成CO2和H2O时提供的ATP少于相同碳原子数的饱和脂肪酸。
酮体(acetonebodies)是脂肪酸在肝脏进行正常分解代谢所生成的特殊中间产物,包括有乙酰乙酸(acetoacetic acid约占30%),β-羟丁酸(β??hydroxybutyric acid约占70%)和极少量的丙酮(acetone)。正常人血液中酮体含量极少(约为0.8?.0mg/dl,0.2??2mM),这是人体利用脂肪氧化供能的正常现象。但在某些生理情况(饥饿、禁食)或病理情况下(如糖尿病),糖的来源或氧化供能障碍,脂动员增强,脂肪酸就成了人体的主要供能物质。若肝中合成酮体的量超过肝外组织利用酮体的能力,二者之间失去平衡,血中浓度就会过高,导致酮血症(acetonemia)和酮尿症(acetonuria)。乙酰乙酸和β-羟丁酸都是酸性物质,因此酮体在体内大量堆积还会引起酸中毒。
1.酮体的生成过程:
酮体是在肝细胞线粒体中生成的,其生成原料是脂肪酸β-氧化生成的乙酰CoA。首先是二分子乙酰CoA在硫解酶作用下脱去一分子辅酶A,生成乙酰乙酰CoA。
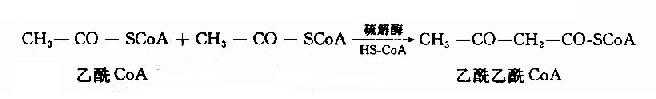
在3-羟-3-甲基戊二酰CoA(hydroxy methyl glutaryl??CoA,HMG??CoA)合成酶催化下,乙酰乙酰CoA再与一分子乙酰CoA反应,生成HMG??CoA,并释放出一分子辅酶。这一步反应是酮体生成的限速步骤。

HMG-CoA裂解酶催化HMG-CoA生成乙酰乙酸和乙酰CoA,后者可再用于酮体的合成。
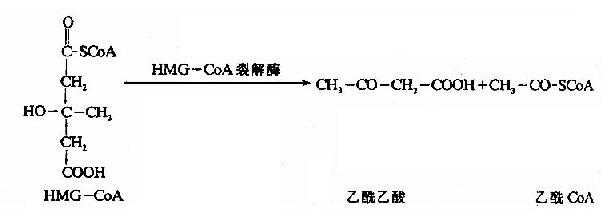
线粒体中的β-羟丁酸脱氢酶催化乙酰乙酸加氢还原(NADH+H+作供氢体),生成β-羟丁酸,此还原速度决定于线粒体中[NADH+H+]/[NAD+]的比值,少量乙栈酸可自行脱羧生成丙酮。

上述酮体生成过程实际上是一个循环过程,又称为雷宁循环(lynen cycle),两个分子乙酰CoA通过此循环生成一分子乙酰乙酸(见图5-12)。

图5-12 肝脏内酮体的生成
酮体生成后迅速透过肝线粒体膜和细胞膜进入血液,转运至肝外组织利用。
2.酮体的利用过程
骨骼肌、心肌和肾脏中有琥珀酰CoA转硫酶(succinyl??Coa thiophorase),在琥珀酰CoA存在时,此酶催化乙酰乙酸活化生成乙酰乙酰CoA。??

心肌、肾脏和脑中还有硫激酶,在有ATP和辅酶T存在时,此酶催化乙酰化酸活化成乙酰乙酰CoA。
经上述两种酶催化生成的乙酰乙酰CoA在硫解酶作用下,分解成两分子乙酰CoA,乙酰CoA主要进入三羧酸循环氧化分解。
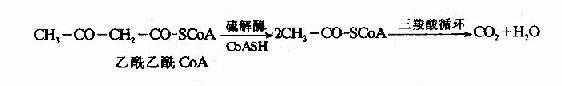
丙酮除随尿排出外,有一部分直接从肺呼出,代谢上不占重要地位,肝外组织利用乙酰乙酸和β-羟丁酸的过程可用下图表示(图5-13)。

图5-13 酮体利用过程
肝细胞中没有琥珀酰CoA转硫酶和乙酰乙酸硫激酶,所以肝细胞不能利用酮体。
肝外组织利用酮体的量与动脉血中酮体浓度成正比,自中酮体浓度达70mg/dl时,肝外组织的利用能力达到饱和。肾酮阈亦为70mg/dl,血中酮体浓度超过此值,酮体经肾小球的滤过量超过肾小管的重吸收能力,出现酮尿症。脑组织利用酮体的能力与血糖水平有关,只有血糖水平降低时才利用酮体。
酮体的生成和利用过程可用下图表示(图5-14)。

图5-14 酮体的生成和利用
3.酮体生成的意义
(1)酮体易运输:长链脂肪酸穿过线粒体内膜需要载体肉毒碱转运,脂肪酸在血中转运需要与白蛋白结合生成脂酸白蛋白,而酮体通过线粒体内膜以及在血中转运并不需要载体。
(2)易利用:脂肪酸活化后进入β-氧化,每经4步反应才能生成一分子乙酰CoA,而乙酰乙酸活化后只需一步反应就可以生成两分子乙酰CoA,β-羟丁酸的利用只比乙酰乙酸多一步氧化反应。因此,可以把酮体看作是脂肪酸在肝脏加工生成的半成品。
(3)节省葡萄糖供脑和红细胞利用:肝外组织利用酮体会生成大量的乙酰CoA,大量乙酰CoA
抑制丙酮酸脱氢酶系活性,限制糖的利用。同时乙酰CoA还能激活丙酮酸羧化酶,促进糖异生。肝外组织利用酮体氧化供能,就减少了对葡萄糖的需求,以保证脑组织、红细胞对葡萄糖的需要。脑组织不能利用长链脂肪酸,但在饥饿时可利用酮体供能,饥饿5?周时酮体供能可多达70%。
(4)肌肉组织利用酮体,可以抑制肌肉蛋白质的分解,防止蛋白质过多消耗,其作用机理尚不清楚。
人体内的脂肪酸大部分来源于食物,为外源性脂肪酸,在体内可通过改造加工被人体利用。同时机体还可以利用糖和蛋白转变为脂肪酸称为内源性脂肪酸,用于甘油三酯的生成,贮存能量。合成脂肪酸的主要器官是肝脏和哺乳期乳腺,另外脂肪组织、肾脏、小肠均可以合成脂肪酸,合成脂肪酸的直接原料是乙酰CoA,消耗ATP和NADPH,首先生成十六碳的软脂酸,经过加工生成人体各种脂肪酸,合成在细胞质中进行。
脂肪酸的合成首先由乙酰CoA开始合成,产物是十六碳的饱和脂肪酸即软酯酸(palmitoleic acid)。
1.乙酰CoA的转移
乙酰CoA可由糖氧化分解或由脂肪酸、酮体和蛋白分解生成,生成乙酰CoA的反应均发生在线粒体中,而脂肪酸的合成部位是胞浆,因此乙酰CoA必须由线粒体转运至胞浆。但是乙酰CoA不能自由通过线粒体膜,需要通过一个称为柠檬酸?脖?酮酸循环(citratepyruvate cycle)来完成乙酰CoA由线粒体到胞浆的转移。首先在线粒体内,乙酰CoA与草酰乙酸经柠檬酸合成酶催化,缩合生成柠檬酸,再由线粒体内膜上相应载体协助进入胞液,在胞液内存在的柠檬酸裂解酶(citrate lyase)可使柠檬酸裂解产生乙酰CoA及草酰乙酸。前者即可用于生成脂肪酸,后者可返回线粒体补充合成柠檬酸时的消耗。但草酰乙酸也不能自由通透线粒体内膜,故必须先经苹果酸脱氢酶催化,还原成苹果酸再经线粒体内膜上的载体转运入线粒体,经氧化后补充草酰乙酸。也可在苹果酸酶作用下,氧化脱羧生成丙酮酸,同时伴有NADPH的生成。丙酮酸可经内膜载体被转运入线粒体内,此时丙酮酸可再羧化转变为草酰乙酸。每经柠檬酸丙酮酸循环一次,可使一分子乙酸CoA由线粒体进入胞液,同时消耗两分子ATP,还为机体提供了NADPH以补充合成反应的需要(见图5-15)。

图5-15 柠檬酸-丙酮酸循环
2.丙二酰CoA的生成
乙酰CoA由乙酰CoA羧化酶(acetyl CoA carboxylase)催化转变成丙二酰CoA(或称丙二酸单酰CoA)反应如下:

乙酰CoA羧化酶存在于胞液中,其辅基为生物素,在反应过程中起到携带和转移羧基的作用。该反应机理类似于其他依赖生物素的羧化反应,如催化丙酮酸羧化成为草酰乙酸的反应等。

图5-16 原核生物脂肪酸合成酶复合物生成软脂酸(16:0)
由乙酰CoA羧化酶催化的反应为脂肪酸合成过程中的限速步骤。此酶为一别构酶,在变构效应剂的作用下,其无活性的单体与有活性的多聚体(由10?0个单体呈线状排列)之间可以互变。柠檬酸与异柠檬酸可促进单体聚合成多聚体,增强酶活性,而长链脂肪酸可加速解聚,从而抑制该酶活性。乙酰CoA羧化酶还可通过依赖于cAMP的磷酸化及去磷酸化修饰来调节酶活性。此酶经磷酸化后活性丧失,如胰高血糖素及肾上腺素等能促进这种磷酸化作用,从而抑制脂肪酸合成;而胰岛素则能促进酶的去磷酸化作用,故可增强乙酰CoA羧化酶活性,加速脂肪酸合成。
同时乙酰CoA羧化酶也是诱导酶,长期高糖低脂饮食能诱导此酶生成,促进脂肪酸合成;反之,高脂低糖饮食能抑制此酶合成,降低脂肪酸的生成。
3.软脂酸的生成
软脂酸的合成实际上是一个重复循环的过程,由1分子乙酰CoA与7分子丙二酰CoA经转移、缩合、加氢、脱水和再加氢重复过程,每一次使碳链延长两个碳,共7次重复,最终生成含十六碳的软脂酸(图5-16)。
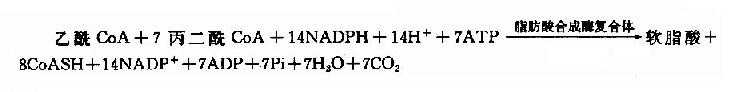
在原核生物(如大肠杆菌中)催化此反应的酶是一个由7种不同功能的酶与一种酰基载体蛋白(acyl carrier protein,ACP)聚合成的复合体。在真核生物催化此反应是一种含有双亚基的酶,每个亚基有7个不同催化功能的结构区和一个相当于ACP的结构区,因此这是一种具有多种功能的酶。
脂肪酸合成需消耗ATP和NADPH+H+,NADPH主要来源于葡萄糖分解的磷酸戊糖途径。此外,苹果酸氧化脱羧也可产生少量NADPH。
脂肪酸合成过程不是β-氧化的逆过程,它们反应的组织,细胞定位,转移载体,酰基载体,限速酶,激活剂,抑制剂,供氢体和受氢体以及反应底物与产物均不相同(表5-6)。
表5-6 脂肪酸合成和分解的比较
| 合成 | 分解 | |
| 反应最活跃时期 | 高糖膳食后 | 饥饿 |
| 刺激激素 | 胰岛素/胰高血糖素高比值 | 胰岛素/胰高血糖素低比值 |
| 主要组织定位 | 肝脏为主 | 肌肉、肝脏 |
| 亚细胞定位 | 胞浆 | 线粒体为主 |
| 酰基载体 | 柠檬酸(线粒体到胞浆) | 肉毒碱(胞浆到线粒体) |
| 含磷酸酰疏基乙胺的活性载体 | 酰基载体蛋白区,CoA | CoA |
| 氧化还原辅因子 | NADPH | NAD+,FAD |
| 二碳供体/产物 | 丙二酰CoA;酰基供体 | 乙酰CoA:产物 |
| 激活剂 抑制剂 | 柠檬酸脂辅酶CoA(抑制乙酰CoA羧化酶) | 丙二酰CoA(抑制肉毒碱酰基转移酶) |
| 反应产物 | 软脂酸 | 乙酰辅酶A |
人体内不仅有软脂酸,还有碳链长短不等的其它脂肪酸,也有各种不饱和脂肪酸,除营养必需脂肪酸依赖食物供应外,其它脂肪酸均可由软脂酸在细胞内加工改造而成。
1.碳链的延长和缩短
脂肪酸碳链的缩短在线粒体中经β-氧化完成,经过一次β-氧化循环就可以减少两个碳原子。
脂肪酸碳链的延长可在滑面内质网和线粒体中经脂肪酸延长酶体系催化完成。
在内质网,软脂酸延长是以丙二酰CoA为二碳单位的供体,由NADPH+H+供氢,亦经缩合脱羧、还原等过程延长碳链,与胞液中脂肪酸合成过程基本相同。但催化反应的酶体系不同,其脂肪酰基不是以ACP为载体,而是与辅酶A相连参加反应。除脑组织外一般以合成硬脂酸(18C)为主,脑组织因含其他酶,故可延长至24碳的脂肪酸,供脑中脂类代谢需要。
在线粒体,软脂酸经线粒体脂肪酸延长酶体系作用,与乙酰CoA缩合逐步延长碳链,其过程与脂肪酸β氧化逆行反应相似,仅烯脂酰CoA还原酶的辅酶为NADPH+H+与β氧化过程不同。通过此种方式一般可延长脂肪酸碳链至24或26碳,但以硬脂酸最多。
2.脂肪酸脱饱和
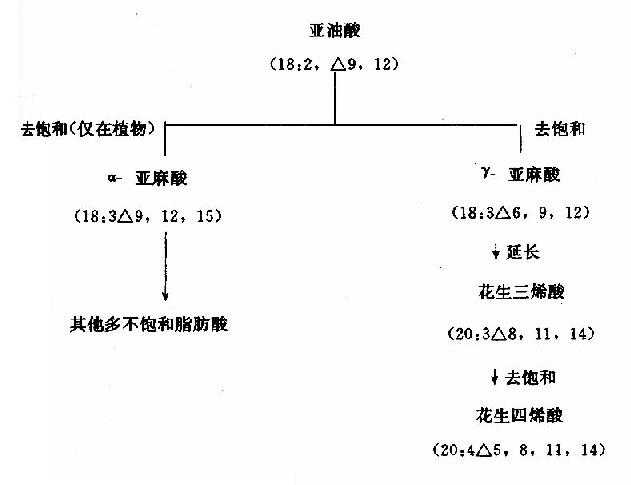
人和动物组织含有的不饱和脂肪酸主要为软油酸(16:1△9)、油酸(18:1△9)、亚油酸(18:2△9,12)、亚麻酸(18:3△9,12,15)、花生四烯酸(20:4△5,8,11,14)等。其中最普通的单不饱和脂肪酸???软油酸和油酸可由相应的脂肪酸活化后经去饱和酶(acylCoAdesaturase)催化脱氢生成。这类酶存在于滑面内质网,属混合功能氧化酶(见肝脏代谢章)。因该酶只催化在△9形成双键,而不能在C10与末端甲基之间形成双键,故亚油酸(linoleate)、亚麻酸(linolenate)及花生四烯酸(arachidonate)在体内不能合成或合成不足。但它们又是机体不可缺少的,所以必须由食物供给,因此,称之为必需脂肪酸(essential fatty acid)。植物组织含有可以在C??10与末端甲基间形成双键(即ω3和ω6)的去饱和酶,能合成以上3种多不饱和脂肪酸。当食入亚油酸后,在动物体内经碳链加长及去饱和后,可生成花生四烯酸。
乙酰CoA羧化酶催化的反应是脂肪酸合成的限速步骤,很多因素都可影响此酶活性,从而使脂肪酸合成速度改变。脂肪酸合成过程中其他酶,如脂肪酸合成酶、柠檬酸裂解酶等亦可被调节。
1.代谢物的调节
在高脂膳食后,或因饥饿导致脂肪动员加强时,细胞内软脂酰CoA增多,可反馈抑制乙酰CoA羧化酶,从而抑制体内脂肪酸合成。而进食糖类,糖代谢加强时,由糖氧化及磷酸戊糖循环提供的乙酰CoA及NADPH增多,这些合成脂肪酸的原料的增多有利于脂肪酸的合成。此外,糖氧化加强的结果,使细胞内ATP增多,进而抑制异柠檬酸脱氢酶,造成异柠檬酸及柠檬酸堆积,在线粒体内膜的相应载体协助下,由线粒体转入胞液,可以别构激活乙酰CoA羧化酶。同时本身也可裂解释放乙酰CoA,增加脂肪酸合成的原料,使脂肪酸合成增加。
2.激素的调节
胰岛素、胰高血糖素、肾上腺素及生长素等均参与对脂肪酸合成的调节。
胰岛素能诱导乙酰CoA羧化酶、脂肪酸合成酶及柠檬酸裂解酶的合成,从而促进脂肪酸的合成。此外,还可通过促进乙酰CoA羧化酶的去磷酸化而使酶活性增强,也使脂肪酸合成加速。
胰高血糖素等可通过增加cAMP,致使乙酰CoA羧化酶磷酸化而降低活性,因此抑制脂肪酸的合成。此外,胰高血糖素也抑制甘油三酯合成,从而增加长链脂酰CoA对乙酰CoA羧化酶的反馈抑制,亦使脂肪酸合成被抑制。
前列腺素(prostaglandin,PG),血栓素(thromboxane,TX)和白三烯(leukotrienes,LT)均由花生四烯酸衍生而来。它们在细胞内生成后,可作为调节物对几乎所有的细胞代谢发挥调节作用,而且与炎症、过敏反应和心血管疾病等病理过程有关。
生物膜上的膜磷脂含有花生四烯酸,它可被磷脂酶A2水解,释放花生四烯酸。花生四烯酸可在前列腺素内过氧化物合成酶催化下,消耗O2和还原性谷胱甘肽,发生氧化和环化反应,生成前列腺素H2。前列腺素H2可进一步衍生成其它前列腺素及血栓素(见图5?7)。可的松(cortisol)抑制磷酸酶A2活性,减少花生四烯酸的生成,从而抑制前列原素的合成,阿斯匹林(aspirin)和保泰松(phenylbutazone)抑制前列腺素内过氧化物合成酶活性使前列腺素和血栓素生成减少。

图5-17 花生四烯酸生成PG,TX和LT概况
PG等在细胞内含量很低,仅10?1pmol/L,但具有很强的生理活性。
血小板产生的TXA2及PGE2促进血小板聚集,血管收缩,促进凝血及血栓形成,而血管内皮细胞释放的PGI2则有很强的舒血管及抗血小板聚集,抑制凝血及血栓形成,与TXA2的作用对抗。北极地区爱斯基摩人摄食富含花生四烯酸的血类食物,能在体内合成PGE3,PGI3及TXA3等三类化合物。PGI3能抑制花生四烯酸从膜磷脂释放,因而抑制PGI2及TXA2的合成。由于PGI3的活性与PGI2相同,而TXA3则较TXA2弱得多,因此爱斯基摩人抗血小板聚集及抗凝血作用较强,被认为是他们不易患心肌梗塞的重要原因之一。
已证实过敏反应的慢反应物质(SRS??A)是LTC4、TD4及LTE4的混合物,其使支气管平滑肌收缩的作用较组胺及PGF2强100000倍,作用缓慢而持久。此外,LTG4还能调节白细胞的功能,促进其游走及趋化作用,刺激腺苷酸环化酶,诱发多核白细胞脱颗粒,使溶酶释放水解酶类,促进炎症及过敏反应的发展。

《生物化学与分子生物学》相关章节:
- ……
- 第五节 血糖及血糖含量调节
- 第五章 脂类代谢
- 第一节 概 述
- 第二节 血脂及其代谢
- 第三节 甘油三酯代谢
- 第四节 脂肪酸代谢(当前内容)
- 第五节 磷脂代谢
- 第六节 胆固醇代谢
- 第六章 生物氧化(Biological oxidation)
- 第一节 概 述
- ……




